Produtos cosméticos

Quem garante a qualidade e segurança dos produtos cosméticos?
Um produto cosmético não é objecto de uma autorização de colocação no mercado, sendo a segurança do produto da inteira responsabilidade do fabricante ou do seu representante legal.
Após o início da sua comercialização, e de modo a garantir que não representam risco para a saúde do consumidor, estes produtos são controlados pela autoridade competente para os produtos cosméticos – Infarmed – sem prejuízo das atribuições e competências legalmente adstritas a outras entidades.
O que deve saber quando adquire um produto cosmético?
¬ Se a rotulagem do produto contém informação sobre o nome e endereço da empresa responsável pelo produto na União Europeia e lista de ingredientes;
¬ Se a rotulagem contém informação em língua portuguesa relativamente a volume/peso, número de lote ou outra referência do produto, função e data de durabilidade mínima, indicada através da expressão "a utilizar de preferência antes de (dia/mês/ano)” ou pelo período após abertura expresso pelo símbolo de caixa aberta, seguido de meses ou ano, bem como precauções de uso, uso exclusivo profissional ou outras advertências.
Circuito dos Produtos Cosméticos
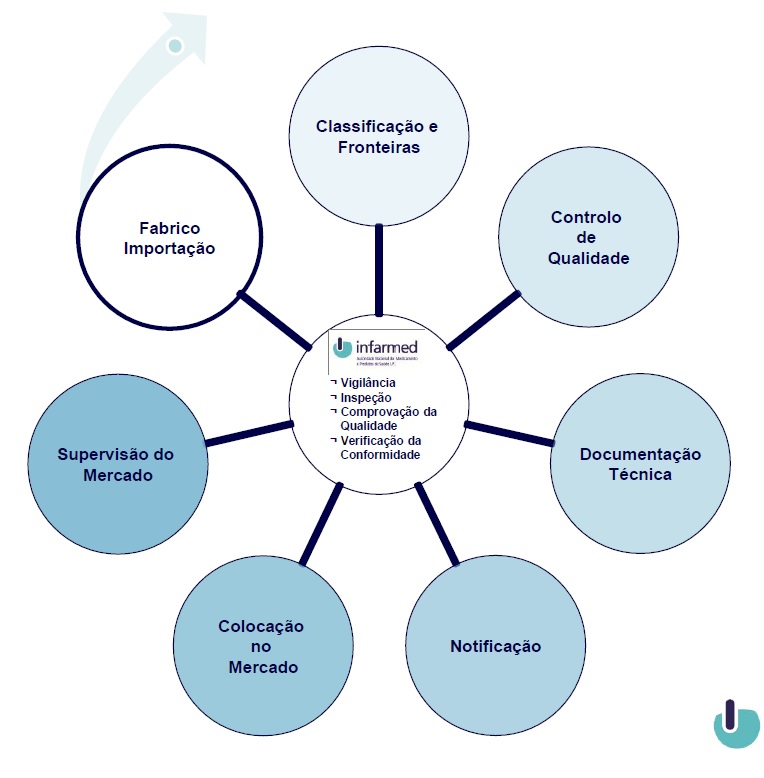
Os produtos cosméticos podem ser fabricados em Portugal, em território de outro estado membro da União Europeia, ou importados de fabricantes sediados em países terceiros.
A importação de produtos cosméticos para colocação no mercado carece de apresentação na autoridade aduaneira, como suporte da declaração aduaneira, do documento de conformidade emitido pelo Infarmed.
Esta obrigatoriedade não é aplicável a importações de produtos cosméticos sem carácter comercial, designadamente, uso pessoal, amostras para análise laboratorial, de rotulagem, de ingredientes ou para efeitos de catálogo.
Classificação e fronteiras de produtos cosméticos
São considerados produtos fronteira aqueles cuja classificação apresenta dúvidas, pela composição, zona de aplicação, rotulagem e menções. Os produtos fronteira devem ser avaliados pela legislação mais exigente e caso a caso.
Por exemplo os produtos fronteira cosmético/medicamento devem ser avaliados pela legislação aplicável a medicamentos.
Exemplos de produtos fronteira:
¬ Produtos para desinfecção das mãos;
¬ Estimulantes de crescimento capilar;
¬ Pastilhas para manter os dentes limpos/mau hálito;
¬ Produtos de peeling.
Documentação técnica de produtos cosméticos
Existe um conjunto de documentos associados a cada cosmético, com especificações técnicas, que devem estar à disposição do Infarmed, num local designado pelo fabricante / importador e no qual devem ser registadas as informações seguintes:
¬ Identificação clara do produto;
¬ Relatório de Segurança;
¬ Processo de fabrico e boas práticas de fabrico e laboratório;
¬ Dados relativos aos ensaios em animais ou métodos alternativos; ¬ Provas dos efeitos reivindicados.
Notificação de produtos cosméticos e colocação no mercado
Os produtos cosméticos colocados no mercado devem ser notificados a cada autoridade competente da União Europeia, ou através do Portal Europeu de Notificação de Produtos Cosméticos (CPNP). A partir de 11 de julho de 2013, a notificação de produtos cosméticos será efectuada exclusivamente através do CPNP.
Até essa data, os produtos cosméticos que não estejam notificados no CPNP devem ser notificados pelos responsáveis pela colocação no mercado nacional ao Centro de Informação Anti-Venenos (CIAV) do Instituto Nacional de Emergência Médica (INEM) e ao Infarmed.
Notificação de produtos cosméticos ao CIAV e ao Infarmed
Ao CIAV devem ser dadas todas as informações adequadas e suficientes acerca das substâncias usadas nos produtos cosméticos para fins de tratamento médico rápido.
Ao Infarmed, no processo de notificação de colocação no mercado, deve ser feito prova de que o CIAV está informado, para poder agir em caso de algum incidente decorrente da utilização de algum produto cosmético.
Verificação da conformidade
As acções de verificação da conformidade dos produtos cosméticos colocados no mercado, incidem sobre a verificação dos requisitos legais e sobre recomendações:
¬ Composição do produto (conservantes, ingredientes proibidos ou com limite de concentração);
¬ Rotulagem (língua portuguesa, informação enganosa, função/apresentação, nome e endereço da pessoa responsável)
¬ Notificação ao CIAV/Infarmed ou CPNP.
Em casos de risco grave para a saúde, ou incumprimento grave, o Infarmed pode suspender, restringir ou retirar o produto cosmético do mercado nacional. Se considerar que o incumprimento não se limita ao território nacional deve acionar o Sistema de Troca Rápida de Informação (RAPEX) do Parlamento Europeu e do Conselho da Europa, de forma a que os estados membros possam agir em conformidade.
Inspecção e comprovação da qualidade
Com o objectivo de garantir a protecção da saúde pública dos consumidores de produtos cosméticos, e no âmbito das actividades de supervisão do mercado, o Infarmed realiza inspecções às entidades que se dediquem ao fabrico, distribuição, armazenagem e venda de produtos cosméticos, podendo colher amostras de cosméticos para controlo e avaliação laboratorial destes produtos, realizados no laboratório de comprovação da qualidade deste instituto, de forma a assegurar que os produtos colocados no mercado estão em cumprimento com a legislação aplicável, protegendo assim os consumidores contra alegações enganosas em relação à eficácia e outras características dos produtos cosméticos.
Cosmetovigilância
O Infarmed é responsável por monitorizar a notificação de efeitos indesejáveis e gerir os riscos relacionados com a utilização dos produtos cosméticos.
É essencial que todos os efeitos indesejáveis detectados decorrentes do uso de produtos cosméticos e de higiene corporal sejam notificados ao Infarmed para que os dados possam ser tratados e se tomem as devidas providências de modo a salvaguardar a segurança dos consumidores.
Os profissionais de saúde, fabricantes, responsáveis pela colocação no mercado e consumidores devem notificar ao Infarmed todos os efeitos indesejáveis graves, ou apesar de menos graves acontecerem num grande número de pessoas, decorrentes da utilização de produtos cosméticos e de higiene corporal. Do estudo destes dados podem resultar acções como alteração das menções na rotulagem, suspensão da comercialização ou retirada do produto do mercado.
O que fazer se ocorrer um efeito indesejável após a utilização de um produto cosmético?
No caso de experienciar um efeito indesejável, o utilizador deverá rapidamente contactar um dermatologista, médico assistente, farmacêutico ou outro profissional de saúde. O produto suspeito deverá ser conservado em seu poder, e disponibilizar ao Infarmed, através do preenchimento da ficha de notificação de efeitos indesejáveis de produtos cosméticos e de higiene corporal (disponível no site do Infarmed), informação pertinente sobre a ocorrência.
Nesta ficha deverão constar, no mínimo, os seguintes dados:
¬ Identificação do notificador;
¬ Descrição detalhada do produto suspeito de ter originado o efeito indesejável;
¬ Caracterização do utilizador (idade, sexo);
¬ Descrição do efeito indesejável.
Nestas circunstâncias poderá também contactar:
Direcção de Produtos de Saúde
Tel.: 21 798 72 64 ou Fax: 21 798 72 81
e-mail: [email protected]
Onde posso obter mais informação sobre produtos cosméticos?
Para informações mais detalhadas e esclarecimentos adicionais sobre o ciclo de vida dos produtos cosméticos, consulte a Linha do Medicamento 800 222 444, que também esclarece sobre produtos de saúde (dispositivos médicos e produtos cosméticos).
